 |
| Percorsi di formazione delle NET. |
Il nuovo meccanismo di morte cellulare attiva coinvolto nell'attività adiuvante dell'alluminio e nelle reazioni avverse indotte dai vaccini contenenti alluminio.
Durante un'infezione, il DNA contenuto nei neutrofili legato a proteine antimicrobiche intracellulari (NET) viene rilasciato nel mezzo extracellulare come mezzo di difesa contro i patogeni (batteri e funghi).
Ovviamente se questo sistema di difesa viene eccessivamente stimolato, il DNA rilasciato rimane troppo a lungo nel mezzo extracellulare e può causare varie patologie (malattie autoimmunitarie/infiammatorie, tumori, vaso-occlusioni ...).
Da studi recenti risulta che uno dei meccanismi che possono spiegare l'efficacia come adiuvante dell'alluminio è la sua capacità di indurre la morte cellulare dei neutrofili (NET-osi) e il rilascio di NET nello spazio extracellulare. La formazione di NET può spiegare anche l'induzione di alcuni dei danni causati dai vaccini che contengono alluminio.
"I neutrofili sono una delle prime linee di difesa contro i microbi invasori. I neutrofili in circolazione sono diretti dalle citochine nei tessuti infetti, dove incontrano i microbi invasori.
Questo incontro porta all'attivazione dei neutrofili e alla fagocitosi [trasporto all'interno della cellula] del patogeno in un fagosoma.
Nel fagosoma i microrganismi sono esposti ad alte concentrazioni di ROS (radicali liberi) e peptidi antimicrobici, responsabili dell'uccisione microbica.
Questo incontro porta all'attivazione dei neutrofili e alla fagocitosi [trasporto all'interno della cellula] del patogeno in un fagosoma.
Nel fagosoma i microrganismi sono esposti ad alte concentrazioni di ROS (radicali liberi) e peptidi antimicrobici, responsabili dell'uccisione microbica.
Recentemente è stato descritto un nuovo meccanismo antimicrobico da parte dei neutrofili. All'attivazione, i neutrofili rilasciano trappole extracellulari (trappole extracellulari di neutrofili [NETs]).
I NET sono composti da cromatina [DNA] associata a proteine granulari.
Queste strutture legano i batteri Gram-positivi e negativi, nonché i funghi. I NET forniscono un'alta concentrazione locale di molecole antimicrobiche che uccidono efficacemente i microbi. I NET sono abbondanti nei siti infiammati, come mostrato per l'appendicite umana e un modello sperimentale di shigellosi. Recentemente, i NET hanno dimostrato di essere rilevanti in vivo nella preeclampsia umana e nelle infezioni da streptococco, causando fascite necrotizzante e polmonite pneumococcica.
I NET sono composti da cromatina [DNA] associata a proteine granulari.
Queste strutture legano i batteri Gram-positivi e negativi, nonché i funghi. I NET forniscono un'alta concentrazione locale di molecole antimicrobiche che uccidono efficacemente i microbi. I NET sono abbondanti nei siti infiammati, come mostrato per l'appendicite umana e un modello sperimentale di shigellosi. Recentemente, i NET hanno dimostrato di essere rilevanti in vivo nella preeclampsia umana e nelle infezioni da streptococco, causando fascite necrotizzante e polmonite pneumococcica.
I neutrofili attivati avviano un processo in cui inizialmente perdono la morfologia nucleare classica. Successivamente, tutte le membrane interne scompaiono, consentendo la miscelazione dei componenti NET. Infine, i NET emergono dalla cellula mentre la membrana citoplasmatica viene rotta da un processo distinto dalla necrosi o dall'apoptosi. In un'infezione, la formazione di ROS può contribuire ai seguenti due percorsi antimicrobici: uccisione intrafagosomale in neutrofili vivi e post mortem (NET-osi) mediata da NET."
https://www.nature.com/articles/nri.2017.105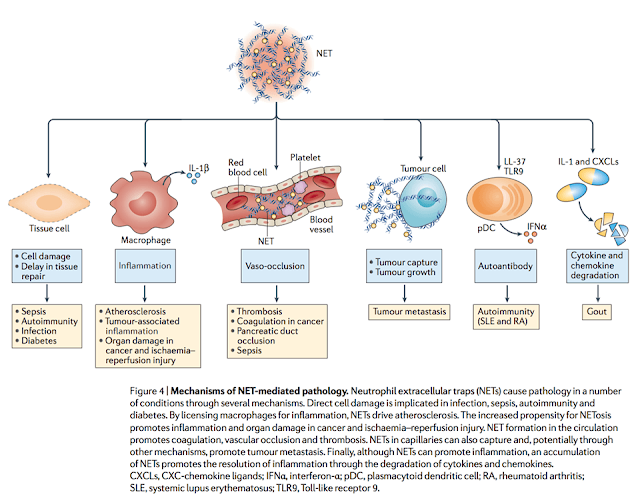 |
| Meccanismi delle patologie NET-mediate |
"Il rilascio del DNA ospite svolge un ruolo fondamentale nella funzione dell'alluminio adiuvante. I neutrofili sono le principali cellule reclutate entro 2 ore dall'iniezione [intramuscolare] dell'alluminio adiuvante.
Da studi di imaging si è potuto confermare che il flusso di neutrofili si concentra sull'alluminio e la morte cellulare dei neutrofili è associata alla presenza di filamenti di DNA all'interno del tessuto dove si trova l'alluminio.
Questi filamenti furono successivamente confermati essere le trappole extracellulari di neutrofili (NET).
Questi studi dimostrano che il meccanismo della morte dei neutrofili svolge un ruolo importante nell'attività adiuvante dell'alluminio e può spiegare come la reazione cellulare nel sito di iniezione determina la liberazione del DNA ospite".
Da studi di imaging si è potuto confermare che il flusso di neutrofili si concentra sull'alluminio e la morte cellulare dei neutrofili è associata alla presenza di filamenti di DNA all'interno del tessuto dove si trova l'alluminio.
Questi filamenti furono successivamente confermati essere le trappole extracellulari di neutrofili (NET).
Questi studi dimostrano che il meccanismo della morte dei neutrofili svolge un ruolo importante nell'attività adiuvante dell'alluminio e può spiegare come la reazione cellulare nel sito di iniezione determina la liberazione del DNA ospite".
